Ciência e Saúde
Bioimpressão 4D

A bioimpressão 4D está a redefinir os limites da medicina regenerativa ao possibilitar a criação de tecidos vivos capazes de se adaptar e evoluir após a impressão.
Nas últimas duas décadas, a engenharia de tecidos tem evoluído de forma notável devido ao desenvolvimento da bioimpressão. Esta tecnologia de elevada precisão permite produzir modelos tridimensionais utilizados em investigação biomédica e ensaios farmacológicos, de modo a reproduzir com maior fidelidade os tecidos humanos. Tem como base a deposição controlada de biotintas, ou seja, de misturas de células vivas e matrizes biocompatíveis, segundo arquiteturas digitais predefinidas.
Da Estática à Dinâmica: Diferenças entre 3D e 4D
A bioimpressão 3D centra-se na reprodução fiel da arquitetura tridimensional de um tecido, permitindo a criação de estruturas estáveis que mantêm a forma e as propriedades definidas no momento da sua produção.
A bioimpressão 4D emerge no contexto da necessidade de desenvolver modelos mais dinâmicos e biomiméticos, capazes de ter em conta a dimensão tempo. Estas estruturas são concebidas para responder a estímulos químicos ou físicos como pH, temperatura ou campos elétricos. Esta capacidade de adaptação possibilita a criação de sistemas que reproduzem com maior fidelidade o dinamismo e a complexidade biológica dos tecidos vivos.
O Ciclo de Produção: Do Digital ao Biológico
A conversão de um modelo digital num tecido funcional é estruturada em três fases fundamentais, seja em bioimpressão 3D quer em 4D.
A primeira fase, o pré-processamento, consiste na elaboração de um modelo digital detalhado, recorrendo a software CAD e a exames de imagem do paciente, como tomografias computadorizadas ou ressonâncias magnéticas. Esta abordagem personalizada garante que o tecido a imprimir reproduza com precisão a anatomia individual, constituindo a base para um resultado altamente específico e funcional.
Segue-se a fase de processamento, correspondente à impressão propriamente dita. Nesta etapa, a impressora deposita de forma controlada as biotintas, camada sobre camada, para construir a arquitetura desejada. Um dos principais desafios reside na preservação da viabilidade celular, assegurando que as células sobrevivam às forças mecânicas, pressões e variações térmicas associadas ao processo.
Por fim, o pós-processamento envolve o cultivo do tecido em biorreatores que fornecem nutrientes e estímulos mecânicos ou elétricos. Este ambiente controlado promove a organização celular, a diferenciação e o início de processos essenciais, como a vascularização, uma condição indispensável para que o tecido atinja plena funcionalidade.
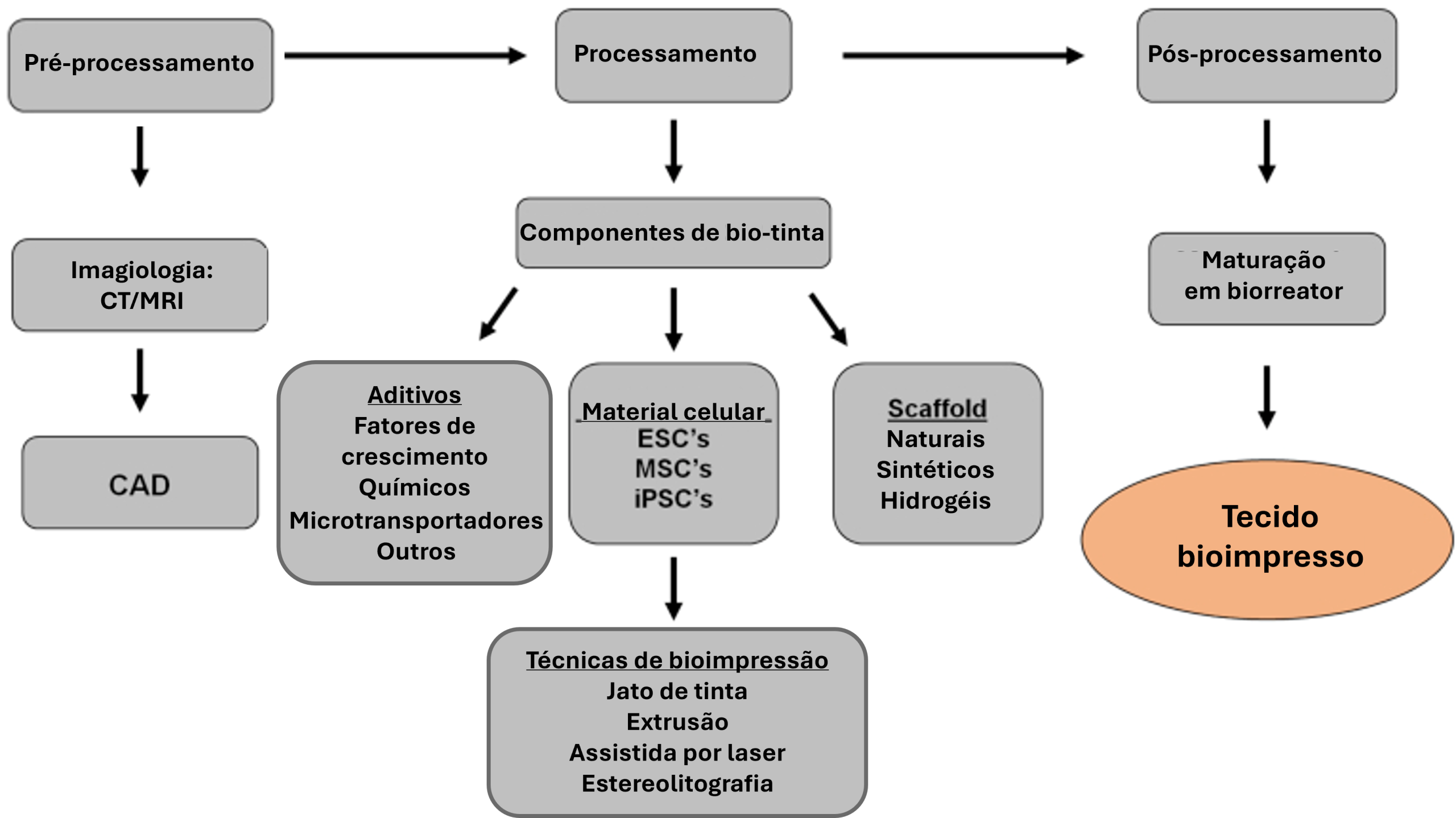
Visão geral esquemática da bioimpressão. Imagem adaptada de “3-D bioprinting technologies in tissue engineering and regenerative medicine: Current and future trends” por E. S. Bishop et al., 2017, Genes & Diseases
Aplicações Clínicas e Investigação
Em engenharia de tecidos ósseos, por exemplo, scaffolds impressos em 4D podem modificar a sua geometria para preencher defeitos complexos, ajustando-se ao local da implantação e promovendo uma melhor integração funcional ao favorecer a regeneração óssea e ao criar microambientes que estimulam o crescimento celular e a osteogénese. Na medicina regenerativa, a utilização de células do próprio paciente para imprimir tecidos, como pele ou cartilagem, reduz significativamente o risco de rejeição imunológica, representando um avanço crucial na área dos transplantes e da reconstrução tecidular. Estes sistemas representam soluções promissoras para defeitos ósseos personalizados e para cirurgia regenerativa.
Em dispositivos médicos adaptativos, destacam-se stents autoajustáveis, oclusores (“occluders”) e microagulhas terapêuticas. Os stents são estruturas implantáveis utilizadas para manter vasos sanguíneos ou outros canais abertos, os oclusores são dispositivos concebidos para a oclusão de defeitos anatómicos, como comunicações anómalas entre cavidades ou vasos, e as microagulhas terapêuticas correspondem a sistemas minimamente invasivos que permitem a administração localizada de fármacos através da pele ou de outros tecidos. Estes têm a capacidade de mudar de forma ou posição após a introdução no organismo, o que permite libertação controlada de fármacos e, consequentemente, melhora a adaptação aos tecidos e abre caminho a implantes programáveis, possibilitando intervenções menos invasivas e mais personalizadas.
A bioimpressão 4D permite igualmente a criação de microambientes celulares tridimensionais controláveis, nos quais o crescimento e a organização celular podem ser ajustados em resposta a estímulos externos. Estes modelos reproduzem de forma mais fiel as condições fisiológicas, permitindo investigar processos biológicos complexos e avaliar terapias com maior realismo e precisão.
Perspetivas futuras
A integração da bioimpressão com gémeos digitais permite que os tecidos impressos sejam planeados e ajustados com base em simulações precisas, facilitando a otimização do desenho do órgão e a previsão de possíveis complicações antes da intervenção clínica.
Outra área em crescimento é a bioimpressão em microgravidade, como na Estação Espacial Internacional, onde a ausência de gravidade facilita a criação de estruturas tridimensionais mais complexas sem suportes adicionais, acelerando o desenvolvimento de tecidos sofisticados e abrindo caminho a aplicações médicas em missões espaciais.
Desafios Éticos
A expansão da bioimpressão para aplicações clínicas levanta desafios éticos e sociais significativos, incluindo questões de segurança, regulamentação e proteção de dados biológicos, dada a natureza sensível das informações envolvidas. A ausência de diretrizes internacionais específicas aumenta a incerteza sobre como integrar estas tecnologias de forma segura e equitativa na prática clínica.
Texto por Sofia I. Conceição Guerreiro. Revisão por Ana Luísa Silva.








